36Kr Japanで提供している記事以外に、スタートアップ企業や中国ビジネスのトレンドに関するニュース、レポート記事、企業データベースなど、有料コンテンツサービス「CONNECTO(コネクト)」を会員限定にお届けします。無料会員向けに公開している内容もあるので、ぜひご登録ください。
原文はこちら
セミナー情報や最新業界レポートを無料でお届け
メールマガジンに登録
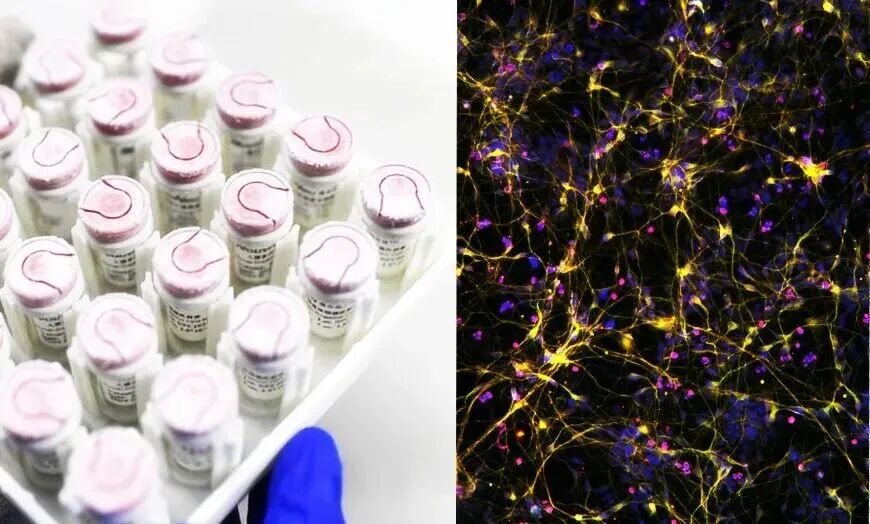
人工多能性幹細胞(iPS細胞、iPSC)由来のパーキンソン病治療薬を開発するスタートアップ企業「睿健医薬(iRegene Therapeutics)」がこのほど追加のシリーズBラウンドで、北極光創投(NLVC)などから資金を調達した。これにより、シリーズBでの計調達額は3億元(約60億円)を超えた。資金は、パーキンソン病治療薬「NouvNeu001」「NouvNeu003」や眼科用剤「NouvSight001」の臨床開発、生産能力の拡大などに用いられる。
2017年に設立された睿健医薬は、iPS細胞に転写因子を導入して分化誘導した医薬品の開発を手がけている。主力製品のNouvNeu001はヒトiPS細胞由来ドーパミン神経前駆細胞で、多施設共同研究の第II相臨床試験を開始した。
創業者の魏君CEOによると、NouvNeu001の第I相臨床試験では、細胞移植から15カ月後の患者で優れた安全性と忍容性が認められた。PET検査でも、免疫抑制剤を使わない状態で、細胞が患者の体内に長期間定着していることが確認された。
NouvNeu001は2025年8月半ばに、米国食品医薬品局(FDA)から優先審査にあたる「ファストトラック(Fast Track)」指定と適用拡大承認を取得。今後はFDAが臨床試験の手法や必要なデータなどについて、同社に対して個別指導を実施する見通しで、臨床応用や商用展開の加速が期待される。
このほか、若年性パーキンソン病患者向け細胞治療薬「NouvNeu003」も独自に開発している。すでに終了した第1相臨床試験では順調にエンドポイントをクリアし、製品の安全性と有効性が予備的に検証された。
投資家である北極光創投の宋高広パートナーは、睿健医薬について「先進的な分化誘導技術プラットフォームと専門チームを基盤に、再生医療分野で大きな進展を遂げている」と評価。特にパーキンソン病治療の開発パイプラインが順調に進展しており、これまでの試験でも極めて高い安全性と有効性が確認されたことから、「米国や日本と肩を並べて競い合える水準に達した」との見方を示した。
*1元=約21円で計算しています。
(翻訳・大谷晶洋)
36Kr Japanで提供している記事以外に、スタートアップ企業や中国ビジネスのトレンドに関するニュース、レポート記事、企業データベースなど、有料コンテンツサービス「CONNECTO(コネクト)」を会員限定にお届けします。無料会員向けに公開している内容もあるので、ぜひご登録ください。
原文はこちら
セミナー情報や最新業界レポートを無料でお届け
メールマガジンに登録










 フォローする
フォローする フォローする
フォローする










